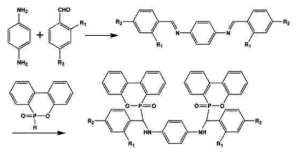
8-羟基喹啉在抗真菌药物研发中的创新应用
发表时间:2025-08-288-羟基喹啉(8-HQ)作为一种具有共轭芳香结构的小分子化合物,其分子中的羟基(-OH)与喹啉环上的氮原子(N)可通过配位作用、氢键作用或疏水作用与生物靶点结合,同时具备一定的脂溶性,能穿透真菌细胞膜,这一特性使其成为抗真菌药物研发的重要母体结构。近年来,基于8-羟基喹啉的结构修饰与功能拓展,在抗真菌药物研发领域涌现出多项创新应用,主要围绕“增强抗真菌活性、拓宽抗菌谱、降低毒副作用、克服耐药性”四大核心目标展开,具体可分为以下方向:
一、金属配合物设计:强化抗真菌作用机制
8-羟基喹啉的喹啉环氮原子与羟基氧原子可与多种金属离子(如锌、铜、铁、镓等)形成稳定的螯合物,这类金属配合物通过“金属离子-配体协同作用”显著提升抗真菌活性,成为当前研发的核心方向之一。
从作用机制来看,一方面,8-羟基喹啉金属配合物可通过“剥夺真菌必需金属离子”发挥作用:真菌生长依赖铁、锌等金属离子参与酶促反应(如细胞呼吸链中的细胞色素氧化酶、核酸合成中的锌指蛋白),它对金属离子的高亲和力可竞争性结合真菌胞内的金属离子,导致其代谢紊乱;另一方面,部分金属离子(如铜离子、镓离子)本身具有氧化应激活性,与8-羟基喹啉结合后,可在真菌胞内诱导活性氧(ROS)生成,破坏细胞膜完整性、氧化蛋白质与核酸,进而实现杀菌效果。
例如,8-羟基喹啉铜配合物(如喹啉铜)已在农业领域用于抗植物真菌病害,近年来研究发现其对人类致病真菌(如白色念珠菌、烟曲霉)同样具有抑制活性:对白色念珠菌的非常小抑菌浓度(MIC)可低至0.5-2μg/mL,且能抑制真菌生物膜的形成 —— 生物膜是真菌耐药的重要原因,该配合物可通过破坏生物膜的 extracellular polymeric substances(EPS)结构,减少真菌黏附与定植。此外,8-羟基喹啉镓配合物因镓离子与铁离子的化学性质相似,可“伪装”进入真菌胞内竞争铁离子结合位点,同时避免对人体正常细胞的毒性(人体细胞对镓离子的摄取率远低于真菌),在抗烟曲霉等丝状真菌感染中展现出良好的选择性,为免疫缺陷患者(如艾滋病患者、化疗患者)的深部真菌感染处理提供了新思路。
二、结构修饰与衍生物合成:优化药代动力学与耐药性
传统8-羟基喹啉类化合物(如氯碘羟喹、羟氯喹)虽具有一定抗真菌活性,但存在水溶性差、口服生物利用度低、长期使用易引发神经系统毒性等问题,且真菌对其耐药性逐渐凸显。通过对 8 - 羟基喹啉的喹啉环、羟基或侧链进行结构修饰,可显著改善其药理性能,这是近年来抗真菌药物研发的重要创新路径。
在结构修饰策略上,主要包括三类:一是在喹啉环的5、7位引入卤素(如氯、溴)或硝基、氨基等基团,增强分子的脂溶性与靶点结合能力 —— 例如,5-氯-7-碘-8-羟基喹啉(氯碘羟喹)的抗真菌活性较母体提升3-5倍,对皮肤癣菌(如红色毛癣菌、须癣毛癣菌)的MIC值可降至0.125μg/mL,且能穿透皮肤角质层,适用于浅部真菌感染(如足癣、体癣)的局部处理;二是在羟基上引入酯基、醚基等亲水性基团,改善水溶性与口服吸收效率 —— 如8-羟基喹啉-2-羧酸乙酯衍生物,其水溶性较母体提升10倍以上,口服后在胃肠道内可缓慢水解释放活性成分,延长作用时间,同时降低对胃肠道黏膜的刺激;三是将8-羟基喹啉与其他抗真菌活性片段(如唑类的咪唑环、多烯类的大环内酯结构)进行拼合,形成“双靶点”或“多靶点”衍生物,克服单一靶点药物的耐药性,例如,将它与氟康唑的三唑环通过亚甲基连接形成的拼合物,可同时抑制真菌的细胞色素P450酶(氟康唑靶点)与金属依赖酶(8-羟基喹啉靶点),对氟康唑耐药的白色念珠菌菌株仍具有强效抑制活性,MIC值较氟康唑降低8-16倍。
三、纳米载体递送系统:提升药物靶向性与生物利用度
8-羟基喹啉及其衍生物的脂溶性差异较大,部分化合物因溶解度低导致生物利用度不足,或因毒性较高限制临床应用。借助纳米载体技术(如脂质体、纳米乳、聚合物纳米粒、金属有机框架(MOFs))对其进行递送,可实现“靶向释药、降低毒副作用、增强抗真菌效果”的目标,成为该类药物研发的重要技术突破方向。
具体而言,纳米载体的优势体现在三方面:一是改善溶解度与稳定性 —— 将8-羟基喹啉包载于聚乳酸-羟基乙酸共聚物(PLGA)纳米粒中,可通过纳米粒的增溶作用提升其水溶性,同时避免药物在体内被酶快速降解,延长半衰期;二是实现靶向递送 —— 通过在纳米载体表面修饰真菌细胞膜特异性受体的配体(如甘露糖、几丁质结合肽),可使药物精准富集于真菌感染部位,减少对正常细胞的损伤,例如,甘露糖修饰的脂质体包载8-羟基喹啉铜配合物,可通过真菌表面的甘露糖受体介导内吞作用进入胞内,对白色念珠菌感染的小鼠模型,其肺部真菌载量较游离药物组降低 2个数量级,且小鼠的存活率提升至80%(游离药物组仅为30%);三是增强药物穿透性 —— 对于深部真菌感染(如真菌性脑膜炎、肝脓肿),纳米载体可通过血脑屏障或穿透脓肿壁,提高病变部位的药物浓度,例如,聚乙二醇(PEG)修饰的8-羟基喹啉纳米乳,其粒径约为100nm,可通过被动靶向作用(EPR效应)富集于肝脏、肺部等感染器官,在真菌性肝脓肿模型中,病灶区药物浓度较游离药物提升5-10倍,显著缩短处理周期。
四、联合用药策略:协同克服真菌耐药
随着抗真菌药物的广泛使用,真菌耐药问题日益严峻(如白色念珠菌对氟康唑的耐药率已超过20%,烟曲霉对伏立康唑的耐药率逐年上升)。8-羟基喹啉及其衍生物因作用机制独特(如干扰金属离子代谢、诱导氧化应激),与传统抗真菌药物(如唑类、多烯类、棘白菌素类)联合使用时,可产生显著的协同抗真菌效应,为耐药真菌感染处理提供新方案。
从协同机制来看,主要包括两类:一是 “靶点互补”—— 例如,8-羟基喹啉与氟康唑联合使用时,氟康唑通过抑制真菌麦角固醇合成(细胞膜关键成分)发挥作用,而它可破坏细胞膜完整性并剥夺金属离子,两者共同作用使真菌细胞膜的损伤加剧,同时抑制真菌的修复机制,对氟康唑耐药菌株的协同指数(FICI)可低至0.125(FICI<0.5为显著协同);二是“逆转耐药性”——部分真菌通过过度表达外排泵(如ABC转运蛋白)将药物排出胞外,导致耐药,8-羟基喹啉可抑制外排泵的ATP酶活性,减少药物外排,提升胞内药物浓度,例如,它与棘白菌素类药物(如卡泊芬净)联合使用时,可使卡泊芬净对耐药烟曲霉的MIC值从8μg/mL降至1μg/mL,同时降低真菌生物膜的耐药性。
此外,8-羟基喹啉与植物源抗真菌成分(如大蒜素、姜黄素)的联合应用也展现出潜力:两者均具有诱导ROS生成的作用,联合使用时可产生“氧化应激叠加效应”,快速破坏真菌细胞结构,且对人体正常细胞的毒性较低,适用于浅部真菌感染的局部处理(如外用凝胶、乳膏)。
本文来源于黄骅市信诺立兴精细化工股份有限公司官网 http://www.xnlxgroup.com/

 ronnie@sinocoalchem.com
ronnie@sinocoalchem.com 15733787306
15733787306